morfologija
Na makroskopskoj razini, kod Alzheimerove bolesti može se uočiti varijabilni stupanj kortikalne atrofije (smanjenje mase tkiva ili organa), karakteriziran povećanjem parijetalnih brazdi, više naglašenih u frontalnom, temporalnom i parijetalnom režnju. Ta se atrofija kompenzira povećanjem ventrikularnih šupljina koje su sekundarne u odnosu na gubitak parenhima (slika 1). Konkretno, u uznapredovalim stadijima bolesti, strukture medijalnog temporalnog režnja, uključujući hipokampus, entorhinalni korteks i amigdalu, ozbiljno atrofiraju, s obzirom na njihovu uključenost počevši od ranih stadija patologije.
Nadalje, Alzheimerova bolest također pokazuje mikroskopske promjene, poznate kao izvanstanični senilni plakovi i unutarstanične neurofibrilarne nakupine, koje predstavljaju osnovu histološke dijagnoze. S progresijom bolesti, postoji ozbiljan gubitak neurona praćen gliozom (ograničena ili difuzna proliferacija, reaktivna u prirodi, neuroglia stanice, tj. Stanice koje čine potpornu stromu živčanog tkiva) u istim regijama. gdje je prisutnost neurofibrilarnih plakova i klastera veća.
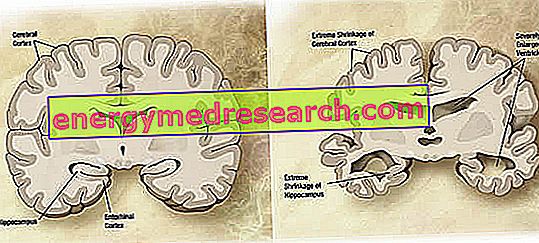
Slika 1. Koronalni dio mozga: razlike između normalnog mozga i mozga koje utječe na AD (izvor slike iz Wikipedije).
patogeneza
Alzheimerovu bolest karakteriziraju uglavnom dvije tipične lezije: ekstracelularna akumulacija senilnih plakova koja se sastoji uglavnom od β-amiloidnog peptida (Ap) i intraneuronskih neurofibrilarnih klastera, formiranih hiperfosforiliranim tau proteinima.
- Senilni plakovi mogu se naći na razini područja mozga kao što su hipokampus, amigdala i neokorteks.
Ap peptid potječe od proteolitičkog rezanja prekursora amiloidnog proteina (APP), s P-sekretazom. Ovaj rez generira terminalni karboksilni fragment od 99 ostataka (CTF ili C99) koji se zatim reže pomoću P-sekretaze kako bi se proizveli fragmenti Ap, koji imaju različite dužine. Poznato je da su najzastupljenije vrste Ap fragment Aβ40. Drugi poznati fragment formiran iz proteolitičkog rezanja, manje bogat od Ap40, je Ap42, skloniji stvaranju amiloidnih fibrila, koje se akumuliraju kao Ap vrste u mozgu pojedinca s Alzheimerovom bolešću.
- Druga komponenta prisutna u Alzheimerovoj bolesti predstavljena je neurofibrilarnim skupinama koje se sastoje od snopova vlakana prisutnih u citoplazmi neurona. Neurofibrilarni klasteri su netopljivi i čini se da su otporni na procese proteolize in vivo, te tako ostaju prisutni u tkivnim presjecima čak i dugo vremena nakon neuronske smrti. Promatrajući strukturu, fibrilarni klasteri sastavljeni su od filamenta dvostruke zavojnice i linearnih filamenata sličnog sastava. Analizirajući sastav, pramenovi dvostrukog heliksa su uglavnom načinjeni od hiperfosforiliranog tau proteina. Tau je aksonski protein povezan s mikrotubulama koji olakšava njegovo sastavljanje.
Druge važne neuropatološke promjene prisutne u Alzheimerovoj bolesti uključuju mitohondrijsku disfunkciju, oksidacijsko neuronsko oštećenje, sinaptički gubitak i degeneraciju aksona.
Neurokemijski aspekti
Kao što je već objašnjeno, peptid Ap, koji potječe od proteolitičkog rezanja prekursora APP, predstavlja neurotoksičnu komponentu Alzheimerove bolesti . Konkretno, pretpostavljeno je da Ap može biti važan za normalne funkcije mozga i, ako prevlada određene koncentracije, može postati neurotoksičan. Osim toga, i agregati i različiti izoformi Ap mogu imati različitu biološku, fiziološku ili patološku ulogu, određivanje i sudjelovanje u kasnijim fazama bolesti. Primijećeno je da Ap djeluje kao neuromodulator, utječući na oslobađanje nekih neurotransmitera u nedostatku očitih znakova neurotoksičnosti.
Na primjer, neuromodulacijska uloga Ap, u fiziološkom kontekstu, mogla bi imati važno značenje za ispravnu ravnotežu neurotransmiterskog sustava. Dobro je poznato da je ovaj sustav sastavljen od neurotransmitera, tvari koje prenose informacije između stanica koje čine živčani sustav, neurone, putem sinaptičkog prijenosa.
U patološkim stanjima, s druge strane, Aβ-posredovana sinaptička transmisija može biti povezana s promjenom neurotransmisije prije neurodegenerativnih događaja. Kao posljedica tih promjena, mogu se pojaviti rani kognitivni i ne-kognitivni poremećaji, temeljeni na zahvaćenim neurotransmiterskim sustavima i različitim uključenim područjima mozga.
Promjene u sustavima neurotransmitera i mehanizmu prijenosa signala u mozgu pojedinaca koji pate od Alzheimerove bolesti vrlo su složeni. Jedan od sustava koji se izgleda mijenja tiče se kolinergičkog signalizacijskog sustava, koji uključuje neurotransmiter acetilkolin. Doista, pokazalo se da pojedinci koji pate od Alzheimerove bolesti pokazuju smanjenu kolinergičku transmisiju na razini korteksa i hipokampusa, važna područja mozga posvećena pojavama kao što su učenje i pamćenje. Uz ovaj sustav neurotransmitera, promjene u noradrenergičkim, serotonergičkim, kao i glutamatnim i GABA sustavima zabilježene su kod Alzheimerove bolesti.



