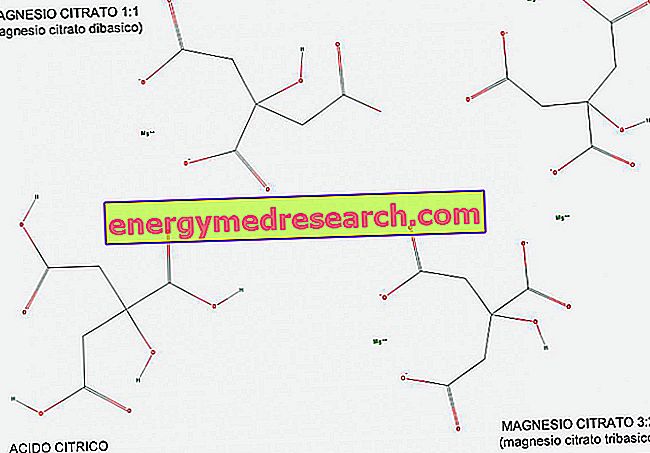
Triazična (ili triprotična) kiselina je kiselina koja ima tri vodikove ione da doniraju u kiselinsko-bazičnoj reakciji. Pomoću slike možemo vidjeti kako je limunska kiselina primjer tribazične kiseline, budući da ima tri COOH karboksilne skupine koje lako prenose vodik H.
Magnezij citrat postoji u omjeru 1: 1 (1 molekula magnezija po molekuli citrata), te u omjeru 3: 2 (3 molekule magnezija na 2 molekule citrata).
1: 1 magnezij citrat se naziva dibaznim, jer je dibazična sol limunske kiseline; u stvari, ona ima 2 jednovalentne osnovne skupine (COO-) po molekuli, izvedene iz 2 karboksilne skupine koje su odvojile svoj vodik tijekom reakcije.
Magnezij 3: 2, s druge strane, naziva se tribazični jer ima 3 jednovalentne osnovne skupine (COO-) po molekuli, izvedene iz 3 karboksilne skupine koje su tijekom reakcije odustale od svog vodika.
Tribazični magnezij citrat je očigledno bogatiji magnezijem (+ 42, 6% po masi) od dibazičnog magnezijevog citrata; štoviše, ona je više alkalizirajuća, jer može prihvatiti tri vodikova iona H + protiv dviju prihvatljivih dibazičnih. Međutim, manje je topljiv u vodi.



